BCI (Synonyms: (E)-BCI) |
| Katalog-Nr.GC38646 |
BCI, als selektiver Dual-spezifischer Phosphatase-6 (DUSP6)-Inhibitor, kann das Tumorwachstum und die Entzündung von Makrophagen hemmen.
Products are for research use only. Not for human use. We do not sell to patients.
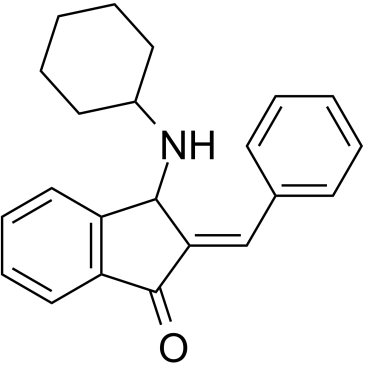
Cas No.: 1245792-51-1
Sample solution is provided at 25 µL, 10mM.
BCI, als selektiver Dual-spezifischer Phosphatase-6 (DUSP6)-Inhibitor, kann das Tumorwachstum und die Entzündung von Makrophagen hemmen.[1].
In vitro zeigte BCI bei niedrigen Dosen von ≤2 μM und ≤4 μM keine zytotoxischen Effekte auf RAW264.7-Zellen bzw. BMMs. Und bei Konzentrationen von ≤4 μM hatte BCI keinen offensichtlichen Einfluss auf den Zellzyklus oder die Apoptose in BMMs.[1] In in vitro Experimenten wurde gezeigt, dass die Behandlung mit 1 μM BCI die Osteoklastogenese durch Hemmung von DUSP6 verstärkte. Darüber hinaus erhöhte BCI die Expression von osteoklastenbezogenen Genen wie NFATC1, C-fos, ACP5 und DC-STAMP.[2] In in vitro Wirksamkeitstests wurde gezeigt, dass die Behandlung mit 4 μM BCI den Anteil an Zellen, die gespaltenes Caspase-3 exprimieren, deutlich erhöhte, und 4 μM BCI verursachte bereits eine umfangreiche Zytotoxizität in KELLY- und IMR-32-Zellen, wobei nur eine Minderheit der LAN-1- und SK-N-AS-Zellen überlebte.[3] In vitro beeinflusste 1 μM BCI nicht die Gesamt-NCC- und NCC-Oberflächenexpression sowie die ERK1/2-Phosphorylierung. Die Behandlung mit 5 μM BCI kann die ERK1/2-Phosphorylierung deutlich erhöhen und die Gesamt-NCC- und NCC-Oberflächenexpression verringern.[5]
In vivo wurden Mäuse fünf aufeinanderfolgende Tage pro Woche mit 10 mg/kg BCI intraperitoneal behandelt, was die AKT-Aktivierung unterdrückte und die Tumorbildung verhinderte.[4] In in vivo Tests wurde gezeigt, dass die Behandlung mit 50, 100 und 200 mg/kg BCI oral im CPDM-Tiermodell die Anzahl der pNrf2-positiven Zellen im parodontalen Gewebe deutlich erhöhte und den Verlust des Alveolarknochens milderte.[6]
References:
[1] Cai C, et al. BCI Suppresses RANKL-Mediated Osteoclastogenesis and Alleviates Ovariectomy-Induced Bone Loss. Front Pharmacol. 2021 Nov 1;12:772540.
[2] Zhang B, et al. DUSP6 expression is associated with osteoporosis through the regulation of osteoclast differentiation via ERK2/Smad2 signaling. Cell Death Dis. 2021 Sep 2;12(9):825.
[3] Thompson EM, et al. The cytotoxic action of BCI is not dependent on its stated DUSP1 or DUSP6 targets in neuroblastoma cells. FEBS Open Bio. 2022 Jul;12(7):1388-1405.
[4] Duan S, et al. Loss of FBXO31-mediated degradation of DUSP6 dysregulates ERK and PI3K-AKT signaling and promotes prostate tumorigenesis. Cell Rep. 2021 Oct 19;37(3):109870.
[5] Feng X, et al. Aldosterone modulates thiazide-sensitive sodium chloride cotransporter abundance via DUSP6-mediated ERK1/2 signaling pathway. Am J Physiol Renal Physiol. 2015 May 15;308(10):F1119-27.
[6] Zhu C, et al. The therapeutic role of baicalein in combating experimental periodontitis with diabetes via Nrf2 antioxidant signaling pathway. J Periodontal Res. 2020 Jun;55(3):381-391.
Average Rating: 5 (Based on Reviews and 7 reference(s) in Google Scholar.)
GLPBIO products are for RESEARCH USE ONLY. Please make sure your review or question is research based.
Required fields are marked with *